Hỗn hợp X gồm Mg và Al. Cho m (g) X tác dụng với HCl dư thu được 0,672l H2 . Mặt khác , cho m (g) X tác dụng với NaOH dư thu được 0,336l H2 . Tính% mỗi kim loại trong hỗn hợp X ban đầu .

Những câu hỏi liên quan
cho 4,48g hỗn hợp X gồm Ba, Al và mg tác dụng hoàn toàn với H2O dư thì thu được 1,792 lit khí H2. Mặt khác khi cho 4,48 g hỗn hợp X tác dụng với dung dịch NaOH dư thì thu được 2,464 lít khí H2 ( các khí ở dktc). Tính thành phần phần trăm khối kluowngj mỗi kim loại có trong hỗn hợp X
Cho 1 lượng hỗn hợp Mg, Al tác dụng với dung dịch HCl dư thu được 10,08l khí H2 (đktc). Mặt khác. cũng lượng hỗn hợp trên tác dụng với dung dịch NaOH dư thì thu được 6,72l H2 (đktc). Tính khối lượng của mỗi kim loại trong hỗn hợp ban đầu đã dùng.
- Xét TN2:
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
0,2<--------------------------------0,3
=> mAl = 0,2.27 = 5,4 (g)
- Xét TN1:
\(n_{H_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,2------------------->0,3
Mg + 2HCl --> MgCl2 + H2
0,15<------------------0,15
=> mMg = 0,15.24 = 3,6 (g)
Đúng 2
Bình luận (0)
Cho một lượng hỗn hợp Mg – Al tác dụng với dung dịch HCl dư thu được 8,96 lít H2. Mặt khác, cho lượng hỗn hợp như trên tác dụng với dung dịch NaOH dư thì thu được 6,72 lít H2. Các thể tích khí đều đo ở đktc.
Tính khối lượng của mỗi kim loại có trong lượng hỗn hợp đã dùng.
Gọi x, y (mol) lần lượt là số mol Mg, Al trong hỗn hợp.
Phương trình phản ứng:
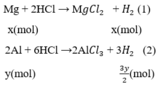
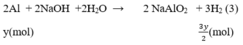
Số mol H2
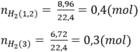
Theo bài ra ta có hệ phương trình:
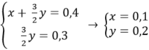
mMg = 24.0,1 = 2,4(g)
mAl = 27.0,2 = 5,4(g)
Đúng 0
Bình luận (0)
Cho một lượng hỗn hợp Mg – Al tác dụng với dung dịch HCl dư thu được 8,96 lít H2. Mặt khác, cho lượng hỗn hợp như trên tác dụng với dung dịch NaOH dư thì thu được 6,72 lít H2. Các thể tích khí đều đo ở đktc. Tính khối lượng của mỗi kim loại có trong lượng hỗn hợp đã dùng.
$2Al + 2H_2O + 2NaOH \to 2NaAlO_2 + 3H_2$
$n_{Al} = \dfrac{2}{3}n_{H_2} = \dfrac{2}{3}. \dfrac{6,72}{22,4} = 0,2(mol)$
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
$Mg + 2HCl \to MgCl_2 + H_2$
$n_{H_2} = \dfrac{3}{2}n_{Al} +n_{Mg}$
$\Rightarrow n_{Mg} = \dfrac{8,96}{22,4} - 0,2.\dfrac{3}{2} = 0,1(mol)$
Suy ra :
$m_{Mg} = 0,1.24 = 2,4(gam) ; m_{Al} = 0,2.27 = 5,4(gam)$
Đúng 1
Bình luận (0)
Hoà tan hết hỗn hợp X gồm Mg, Al, Al2O3 tác dụng với dd NaOH dư thu được 0.15 mol H2. Nếu cũng cho hỗn hợp X trên tác dụng hết với HCl thì thu được 0,35 mol H2. Sô mol Mg và Al trong hỗn hợp X theo thứ tự là bao nhiêu ?
$2Al + 2NaOH + 2H_2O \to 2NaAlO_2 + 3H_2$
$n_{Al} = \dfrac{2}{3}n_{H_2} = \dfrac{2}{3}.0,15 = 0,1(mol)$
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
$Mg + 2HCl \to MgCl_2 + H_2$
$n_{H_2} = \dfrac{3}{2}n_{Al} + n_{Mg} = 0,35(mol)$
$\Rightarrow n_{Mg} = 0,35 - 0,15 = 0,2(mol)$
Vậy số mol Mg và Al là 0,2 và 0,1
Đúng 2
Bình luận (0)
Cho 11,8 gam hỗn hợp X gồm Cu và Al tác dụng với dung dịch HCl dư, thu được 6,72 lít H2 (ở đktc). a) Tính % khối lượng mỗi kim loại trong hỗn hợp X ban đầu. b) Tính thể tích dung dịch HCl 20% (d= 1,1 g/ml) đã dùng, biết người ta đã dùng dư 10% so với lượng cần thiết.
Tham khảo
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
0,2----------------------------------------------0,3
nH2=6,72\22,4=0,3 mol
=>mAl=0,2.27=5,4g
Đúng 1
Bình luận (2)
Hỗn hợp X gồm các chất: phenol, axit axetic, etyl axetat. Cho m gam X tác dụng vừa đủ với 300 ml dung dịch NaOH 1M, thu được dung dịch Y. Mặt khác, cho m gam X tác dụng với kim loại K dư thì thu được 2,464 lít khí H2 (đktc). Khối lượng muối trong Y lớn hơn khối lượng hỗn hợp X ban đầu là: A. 5,32 gam B. 4,36 gam. C. 4,98 gam. D. 4,84 gam
Đọc tiếp
Hỗn hợp X gồm các chất: phenol, axit axetic, etyl axetat. Cho m gam X tác dụng vừa đủ với 300 ml dung dịch NaOH 1M, thu được dung dịch Y. Mặt khác, cho m gam X tác dụng với kim loại K dư thì thu được 2,464 lít khí H2 (đktc). Khối lượng muối trong Y lớn hơn khối lượng hỗn hợp X ban đầu là:
A. 5,32 gam
B. 4,36 gam.
C. 4,98 gam.
D. 4,84 gam
Chọn B.
Ta có: n H 2 = 2 , 464 22 , 4 = 0 , 11 m o l
Chỉ có phenol và axit axetic mới phản ứng được với K nên:
C 6 H 5 O H C H 3 C O O H → + K 1 2 H 2
22 mol ← 0,11 mol
Khi cho X tác dụng với NaOH thì cả 3 chất đều tác dụng với NaOH theo tỉ lệ mol 1:1, nghĩa là:
n X = n N a O H = 0 , 3 m o l
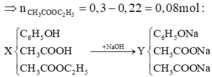
Theo sơ đồ trên ta thấy:
+ Đối với 2 chất đầu từ X đến Y chỉ thay 1 H bằng 1 Na nên khối lượng tăng: 22.0,22 gam.
+ Chất sau thay C2H5 bằng Na nên khối lượng giảm: (29 - 23).0,08 gam
=>mY - mX = 22.0,22 - (29 - 23).0,08 = 4,36 gam
Đúng 0
Bình luận (0)
Hỗn hợp X gồm các chất: phenol, axit axetic, etyl axetat. Cho m gam X tác dụng vừa đủ với 300 ml dung dịch NaOH 1M, thu được dung dịch Y. Mặt khác, cho m gam X tác dụng với kim loại K dư thì thu được 2,464 lít khí H2 (đktc). Khối lượng muối trong Y lớn hơn khối lượng hỗn hợp X ban đầu là: A. 5,32 gam. B. 4,36 gam. C. 4,98 gam. D. 4,84 gam.
Đọc tiếp
Hỗn hợp X gồm các chất: phenol, axit axetic, etyl axetat. Cho m gam X tác dụng vừa đủ với 300 ml dung dịch NaOH 1M, thu được dung dịch Y. Mặt khác, cho m gam X tác dụng với kim loại K dư thì thu được 2,464 lít khí H2 (đktc). Khối lượng muối trong Y lớn hơn khối lượng hỗn hợp X ban đầu là:
A. 5,32 gam.
B. 4,36 gam.
C. 4,98 gam.
D. 4,84 gam.
cho hỗn hợp x gồm al,Mg,Zn 15g x tác dụng với H2SO4 loãng dư thu được 8,96 lit H2. 15g x tác dụng với O2 dư thu đc m g hh Oxit. Tính m
\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Gọi số mol O2 pư là x (mol)
2H+1 + 2e --> H20
0,8<--0,4
O20 + 4e --> 2O-2
x---->4x
=> 4x = 0,8
=> x = 0,2 (mol)
=> m = 15 + 0,2.32 = 21,4 (g)
Đúng 2
Bình luận (0)



















